世界の酵素阻害剤市場:製品タイプ別(ACE阻害剤、HMG-CoA還元酵素阻害剤、ポリメラーゼ阻害剤)、投与経路別(静脈内、経口)、流通チャネル別、適応症別、エンドユーザー別 – グローバル予測 2025年~2032年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
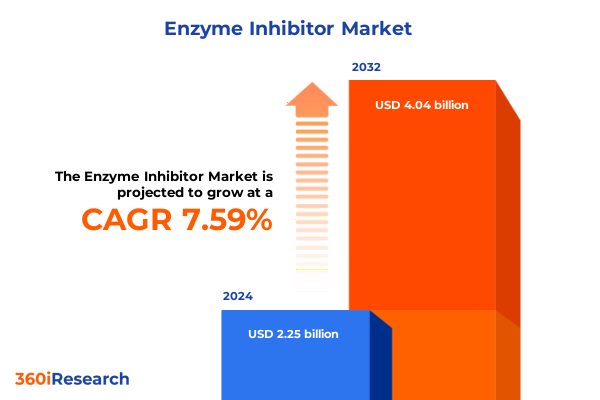
酵素阻害剤市場は、2024年に22.5億米ドルと推定され、2025年には24.0億米ドルに達し、2032年までに年平均成長率(CAGR)7.59%で40.4億米ドルに成長すると予測されています。酵素阻害剤は、現代薬理学の中心に位置し、多様な疾患に関与する生物学的経路を精密に調節するメカニズムを提供します。過去数十年にわたり、これらの特殊な分子は、心血管疾患治療、腫瘍学、感染症管理などにおいて、基本的な研究対象から基盤となる治療法へと進化してきました。酵素活性を選択的に減衰またはブロックする能力は、疾患介入への標的アプローチを可能にし、多くの場合、有効性の向上とオフターゲット効果の低減をもたらします。その結果、酵素阻害剤は治療パラダイムを再定義し、新たな治療領域へと拡大し続けています。この急速な革新を背景に、バイオ医薬品企業、研究機関、医療システムなどのステークホルダーは、酵素阻害剤市場を形成する力学に関する包括的な洞察をますます求めています。本報告書は、市場の現状、主要な推進要因、および将来の展望を詳細に分析し、エビデンスに基づいた意思決定を支援する重要な情報を提供します。
近年、酵素阻害剤のエコシステムを集合的に再構築する画期的な進歩が目撃されています。分子生物学および構造生化学におけるブレークスルーは、高解像度の酵素構造をもたらし、前例のない選択性と効力を持つ阻害剤の設計を促進しました。同時に、創薬ワークフローへの人工知能(AI)と機械学習(ML)の統合は、ヒット化合物の特定とリード最適化を加速させ、開発期間を数年から数ヶ月に短縮しています。さらに、精密医療イニシアチブの台頭は、標的阻害剤とコンパニオン診断薬の共同開発を推進してきました。この組み合わせにより、治療法が最も反応性の高い患者サブセットに確実に届き、臨床転帰を改善し、個別化された治療の価値提案を強化しています。一方、製剤科学の進歩は、経口バイオアベイラビリティの従来の限界を克服し、より便利な投与レジメンを可能にしています。これらの革新は、酵素阻害剤の治療範囲を拡大するだけでなく、データ駆動型創薬と患者中心の開発モデルを採用する組織に競争上の優位性をもたらしています。
詳細なセグメンテーション分析は、酵素阻害剤の開発において製品タイプが重要な差別化要因であることを示しています。ACE阻害剤、HMG-CoA還元酵素阻害剤、ポリメラーゼ阻害剤、プロテアーゼ阻害剤、チロシンキナーゼ阻害剤などのカテゴリーは、それぞれ独自の価値提案と競争環境を示しています。ACE阻害剤セグメント内では、カプトプリル、エナラプリル、リシノプリルなどの分子が心血管管理における基本的な治療法として機能し続けていますが、新興のジェネリック医薬品や配合剤が競争を激化させています。適応症別に見ると、酵素阻害剤は心血管疾患、感染症、代謝性疾患、神経学、腫瘍学において異なる軌跡を示しています。心不全、高血圧、心筋梗塞は心血管阻害剤の焦点であり続ける一方、C型肝炎やHIVはポリメラーゼ阻害剤およびプロテアーゼ阻害剤クラスの革新を推進しています。代謝性疾患では、糖尿病や肥満が満たされていない高いニーズを提示し、新規製剤や併用療法を刺激しています。同様に、アルツハイマー病やパーキンソン病、乳がん、結腸直腸がん、肺がんをカバーする神経学および腫瘍学分野は、血液脳関門を通過したり、特定のキナーゼを阻害したりするように設計された標的阻害剤から恩恵を受けています。投与経路を考慮すると、患者の利便性から経口製剤が優勢であり、カプセル、経口溶液、錠剤はバイオアベイラビリティと用量精度に最適化されています。静脈内投与オプションは、迅速な発現が不可欠な急性期医療現場でその関連性を維持しています。流通チャネルは市場をさらに細分化し、病院薬局、小売店、オンラインプラットフォームがそれぞれアクセス、在庫管理、患者リーチの点で明確な利点を提供します。最後に、診療所や在宅医療提供者から病院に至るエンドユーザーは、カスタマイズされた提供モードとサポートサービスを要求し、製造業者のエンゲージメント戦略と患者アドヒアランスプログラムに影響を与えています。
地域動向は酵素阻害剤の利用に深い影響を与え、アメリカ、欧州・中東・アフリカ(EMEA)、アジア太平洋の各地域が独自の市場推進要因を提示しています。アメリカでは、堅牢な研究開発インフラと進歩的な償還制度が、次世代阻害剤の迅速な採用を促進しています。北米の主要ハブは臨床試験と規制当局の承認を主導する一方、ラテンアメリカ市場は患者アクセスを拡大するためにジェネリック医薬品やバイオシミラーの参入をますます受け入れています。EMEA内では、多様な医療システムが複雑な償還地域を支えています。西ヨーロッパの厳格な価格統制とHTA評価は、製造業者に明確な価値提案を実証することを強いる一方、中東およびアフリカの新興市場は、手頃な価格と供給の安定性を優先します。地域規制機関間の協力的なイニシアチブは、承認プロセスを合理化し、中段階パイプライン参入者への新たな道を開いています。アジア太平洋地域は、人口規模、疾病負担の増加、および現地生産に対する政府のインセンティブによって推進されるダイナミックな成長フロンティアを構成しています。中国、インド、日本、韓国などの国々は、自国の医薬品開発を加速させるためにバイオテクノロジー・クラスターに多額の投資を行っています。さらに、主要市場における特許切れは、ジェネリック医薬品およびバイオシミラーのライセンス契約の急増を触媒し、酵素阻害剤の状況における競争力学を再形成しています。
主要な製薬およびバイオテクノロジー企業は、多様な革新と協力戦略を通じて酵素阻害剤の軌道を積極的に形成しています。ファイザーは、複雑な疾患経路に対処する多標的阻害剤に焦点を当て、小分子ポートフォリオを拡大し続けています。メルクのパイプラインは、免疫腫瘍学の組み合わせを重視し、プロテアーゼ阻害剤とチェックポイントモジュレーターを統合して抗腫瘍効果を高めています。ロシュは、診断の専門知識を活用して、EGFRおよびBCR-ABL阻害剤とコンパニオンアッセイを共同開発し、精密医療の提供を強化しています。ギリアドのウイルス感染症向けポリメラーゼ阻害剤におけるリーダーシップは継続しており、より広範な抗ウイルス活性を持つ次世代ヌクレオシド類似体を模索しています。一方、ブリストル・マイヤーズ スクイブは、新規チロシンキナーゼ足場にアクセスするための戦略的パートナーシップを追求し、新興の腫瘍学セグメントへの参入を加速させています。アッヴィは、代謝性疾患治療における存在感を確立した後、中枢神経系酵素を標的とする阻害剤をライセンス供与することで神経学分野への多様化を図っています。これらの活動全体を通じて、企業は内部の研究開発投資と、治療パイプラインを最適化するための標的を絞った買収およびライセンス契約とのバランスを取っています。
市場の課題としては、2025年に米国で実施される新たな関税措置が、医薬品原料および原薬(API)に影響を与え、酵素阻害剤のサプライチェーンとコストダイナミクスに複合的な影響を及ぼしています。APIコストの上昇は、製薬企業に調達戦略の見直しとサプライヤーネットワークの多様化を促し、単一地域への依存リスクを軽減させています。これにより、一部の大手バイオ医薬品企業は、国内生産施設への投資やアジアの小規模APIメーカーとの戦略的パートナーシップを加速させています。規制の複雑さも増しており、企業は製品認証、コンプライアンス監査、潜在的な供給途絶に対処する必要があります。これに対応するため、業界リーダーはサプライチェーンの透明性と回復力イニシアチブを優先し、デジタル追跡プラットフォームやニアソーシングモデルを活用しています。
激化する競争と進化する規制環境の中で成功するためには、業界リーダーは俊敏性と革新性を高める実用的な戦略を採用する必要があります。第一に、学術機関やバイオテクノロジー新興企業との共同研究パートナーシップを優先することで、新規酵素標的を発見し、初期段階の発見を加速させることができます。競合前のデータを共有し、外部の専門知識を活用することで、組織は研究開発リスクを分散しながら、臨床までの時間を短縮できます。第二に、製造ネットワークを多様化し、受託開発製造組織(CDMO)に投資することは、世界的な政策変動に直面した際のサプライチェーンの回復力を強化します。APIのニアソーシングとデジタル追跡システムの導入は、継続性と透明性を保証します。第三に、遠隔患者モニタリングやアドヒアランスアプリなどのデジタルヘルスソリューションを製品提供に組み込むことは、患者エンゲージメントと実世界エビデンスの生成を強化し、支払者との価値ベースの契約を支援します。最後に、バイオマーカー駆動型承認や迅速承認経路に関する進化するガイダンスに対応するため、規制当局と積極的に関与することは、競争上の優位性を確保できます。治験デザインと安全性要件に関する早期の対話は、承認の不確実性を低減します。これらの的を絞ったイニシアチブは、企業が新たな治療ニッチを活用し、ライフサイクル管理を最適化し、患者に有意義な成果をもたらすための位置付けを可能にします。
以下に、目次を日本語に翻訳し、詳細な階層構造で示します。
—
**目次**
**I. 序文**
* 市場セグメンテーションとカバレッジ
* 調査対象期間
* 通貨
* 言語
* ステークホルダー
**II. 調査方法**
**III. エグゼクティブサマリー**
**IV. 市場概要**
**V. 市場インサイト**
* オンコロジーにおける新規**酵素阻害剤**標的を特定するためのCRISPRベーススクリーニングの活用
* 有効性向上のためのキナーゼおよびプロテアーゼ阻害を組み合わせたデュアルアクション**酵素阻害剤**の開発
* **酵素阻害剤**リード化合物の設計と最適化における人工知能の統合
* 阻害剤の選択性と安全性プロファイルを高めるための可逆的共有結合戦略の採用
* 腸内マイクロバイオーム調節研究を通じた代謝性疾患治療における**酵素阻害剤**応用の拡大
**VI. 2025年米国関税の累積的影響**
**VII. 2025年人工知能の累積的影響**
**VIII. 酵素阻害剤市場:製品タイプ別**
* ACE阻害剤
* カプトプリル
* エナラプリル
* リシノプリル
* HMG-CoA還元酵素阻害剤
* アトルバスタチン
* ロスバスタチン
* シンバスタチン
* ポリメラーゼ阻害剤
* 非ヌクレオシド系ポリメラーゼ阻害剤
* ヌクレオシド類似体ポリメラーゼ阻害剤
* プロテアーゼ阻害剤
* C型肝炎プロテアーゼ阻害剤
* HIVプロテアーゼ阻害剤
* チロシンキナーゼ阻害剤
* BCR-ABL阻害剤
* EGFR阻害剤
* 第一世代阻害剤
* 第二世代阻害剤
* 第三世代阻害剤
* VEGFR阻害剤
**IX. 酵素阻害剤市場:投与経路別**
* 静脈内
* 経口
* カプセル
* 経口液剤
* 錠剤
**X. 酵素阻害剤市場:流通チャネル別**
* 病院薬局
* オンライン薬局
* 小売薬局
**XI. 酵素阻害剤市場:適応症別**
* 心血管疾患
* 心不全
* 高血圧
* 心筋梗塞
* 感染症
* C型肝炎
* HIV
* 代謝性疾患
* 糖尿病
* 肥満
* 神経学
* アルツハイマー病
* パーキンソン病
* 腫瘍学
* 乳がん
* 結腸直腸がん
* 肺がん
* 非小細胞肺がん
* 小細胞肺がん
* 前立腺がん
**XII. 酵素阻害剤市場:エンドユーザー別**
* 診療所
* 在宅医療
* 病院
**XIII. 酵素阻害剤市場:地域別**
* アメリカ
* 北米
* ラテンアメリカ
* ヨーロッパ、中東、アフリカ
* ヨーロッパ
* 中東
* アフリカ
* アジア太平洋
**XIV. 酵素阻害剤市場:グループ別**
* ASEAN
* GCC
* 欧州連合
* BRICS
* G7
* NATO
**XV. 酵素阻害剤市場:国別**
* 米国
* カナダ
* メキシコ
* ブラジル
* 英国
* ドイツ
* フランス
* ロシア
* イタリア
* スペイン
* 中国
* インド
* 日本
* オーストラリア
* 韓国
**XVI. 競争環境**
* 市場シェア分析、2024年
* FPNVポジショニングマトリックス、2024年
* 競合分析
* AB Enzymes GmbH
* AbbVie Inc.
* Advanced Enzyme Technologies Ltd.
* Amano Enzyme Inc.
* Amgen Inc.
* AstraZeneca PLC
* BASF SE
* Bayer AG
* Boehringer Ingelheim GmbH
* Bristol Myers Squibb Company
* DSM N.V.
* Eli Lilly and Company
* F. Hoffmann-La Roche AG
* GlaxoSmithKline PLC
* Merck & Co., Inc.
* Novartis AG
* Novozymes A/S
* Pfizer Inc.
* Takeda Pharmaceutical Company Limited
**XVII. 図目次 [合計: 30]**
**XVIII. 表目次 [合計: 1431]**
………… (以下省略)
*** 本調査レポートに関するお問い合わせ ***

酵素阻害剤とは、酵素の触媒活性を特異的に低下させる、あるいは完全に停止させる分子群を指す。生体内における酵素反応は生命活動の根幹をなし、その活性の精密な制御は、代謝経路の調節、細胞シグナル伝達、遺伝子発現など、あらゆる生命現象において不可欠である。酵素阻害剤は、この酵素活性制御機構の一翼を担うだけでなく、生物学研究における分子プローブ、さらには医薬品開発における重要なターゲット分子として、その多岐にわたる役割が認識されている。
これらの分子は、酵素の特定の部位に結合することで、その立体構造を変化させたり、基質との結合を妨げたり、あるいは触媒反応そのものを阻害したりする。阻害の様式は大きく可逆的阻害と不可逆的阻害に分類される。可逆的阻害剤は酵素と非共有結合的に結合し、その結合は解離可能であるため、阻害剤濃度が低下すれば酵素活性は回復する。一方、不可逆的阻害剤は酵素と共有結合を形成し、酵素の構造を恒久的に変化させることで、その活性を不可逆的に失わせる。
可逆的阻害には、さらにいくつかのサブタイプが存在する。競合的阻害は、阻害剤が基質と活性部位を奪い合う形で結合し、基質濃度を高めることで阻害効果を克服できる特徴を持つ。非競合的阻害剤は、活性部位以外の部位(アロステリック部位)に結合し、酵素の立体構造を変化させることで触媒効率を低下させるため、基質濃度を上げても阻害効果は解消されない。また、不競合的阻害は、酵素が基質と結合して形成された酵素-基質複合体にのみ阻害剤が結合する特殊な様式である。これらの違いは、阻害剤の作用機序を理解し、その効果を予測する上で極めて重要となる。
生体内では、酵素阻害剤は生理的な調節因子として重要な役割を果たす。例えば、代謝経路の最終産物がその経路の初期段階の酵素を阻害するフィードバック阻害は、過剰な産物の生成を防ぎ、代謝のバランスを維持する上で不可欠な機構である。一方で、酵素阻害剤の中には、生物にとって有害な毒物として作用するものも存在する。神経ガスとして知られる有機リン化合物は、神経伝達物質アセチルコリンを分解するアセチルコリンエステラーゼを不可逆的に阻害し、神経系の機能不全を引き起こす。また、シアン化合物は、細胞呼吸に関わるシトクロムcオキシダーゼを阻害することで、ATP産生を停止させ、生命活動を脅かす。
酵素阻害剤の最も顕著な応用分野の一つは、医薬品開発である。特定の疾患の原因となる酵素の活性を特異的に阻害することで、その疾患の進行を抑制したり、症状を緩和したりする薬剤が数多く開発されてきた。高血圧治療薬のACE阻害薬はアンジオテンシン変換酵素を、高脂血症治療薬のスタチン系薬剤はHMG-CoA還元酵素を阻害する。非ステロイド性抗炎症薬(NSAIDs)はシクロオキシゲナーゼ(COX)を、HIV感染症治療薬のプロテアーゼ阻害剤はウイルスのプロテアーゼを標的とする。がん治療における分子標的薬や、細菌特有の酵素を阻害する抗菌薬もその例であり、酵素阻害剤は現代医療において不可欠な存在となっている。
酵素阻害剤の開発は、その特異性、有効性、そして副作用のバランスを考慮する必要があるため、常に挑戦を伴う。標的以外の酵素に対するオフターゲット効果は、望ましくない副作用の原因となる。また、薬剤耐性の出現は、特に感染症やがん治療において深刻な問題であり、新たな阻害剤の開発を継続的に要求する。近年では、構造生物学、計算化学、ハイスループットスクリーニングといった先端技術を駆使し、より高選択的で強力な阻害剤を合理的に設計するアプローチが主流となっている。
酵素阻害剤は、生命現象の理解を深めるための強力な研究ツールであると同時に、様々な疾患に対する治療薬として人類の健康に多大な貢献をしてきた。その作用機序の多様性、生物学的・薬理学的重要性は計り知れず、今後も新たな疾患の克服や生命科学の発展において、その役割は一層拡大していくことだろう。