世界のCHO細胞株開発サービス市場:サービスタイプ別(細胞株特性解析、クローン選別、遺伝子工学)、発現技術別(人工染色体技術、ランダム挿入、部位特異的挿入)、ビジネスモデル、エンドユーザー、用途 – グローバル予測 2025年~2032年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
## CHO細胞株開発サービス市場:詳細分析(市場概要、推進要因、展望)
### 市場概要
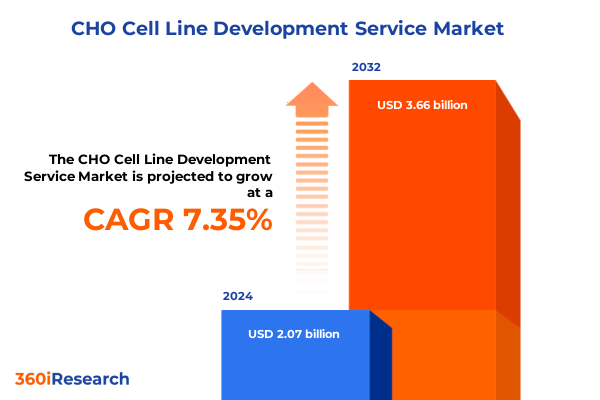
CHO細胞株開発サービス市場は、バイオ医薬品製造の基盤として極めて重要な役割を担っており、モノクローナル抗体、組換えタンパク質、ワクチンといった画期的な治療薬の創出を支えています。2024年には20.7億米ドルと推定された市場規模は、2025年には21.8億米ドルに達し、2032年までに年平均成長率(CAGR)7.35%で36.6億米ドルに拡大すると予測されています。製薬企業やバイオテクノロジー企業が、高品質なバイオ医薬品に対する需要の高まりに応えようと努める中で、チャイニーズハムスター卵巣(CHO)細胞の選択と最適化は、プロセス効率、収量、および規制遵守の決定的な要因となっています。高度な遺伝子工学技術と厳格なスクリーニングプロトコルを活用することで、研究機関や受託サービスプロバイダーは、優れた生産性、安定性、安全性プロファイルを示す細胞株を達成することが可能です。この市場は、技術革新、規制の変化、セグメンテーションの多様性、地域ごとのダイナミクスによって大きく変革されており、業界リーダーは技術的および運用上の卓越性を維持するための戦略を採用しています。
### 推進要因
CHO細胞株開発サービスの市場成長は、主に以下の要因によって推進されています。
**1. 技術革新と自動化の進展:**
遺伝子工学、自動化、データ解析における進歩が、CHO細胞株開発の様相を大きく変えています。CRISPR-CasシステムやCre-Lox組換えなどの部位特異的組込み技術は、標的遺伝子挿入を可能にし、予測可能な性能特性と位置効果の低減を実現するクローンをもたらしています。同時に、スクリーニングのスループット向上とデータ分析の進化により、数千もの候補を並行して評価し、これまでにない速さで最高の性能を持つクローンを特定できるようになりました。次世代のプラットフォームは、ゲノムシーケンシング、高コンテンツイメージング、バイオインフォマティクスパイプラインを組み合わせることで、堅牢なデータセットを生成し、厳格なコンプライアンス要件を満たしています。さらに、クローン選択ワークフローへの人工知能(AI)と機械学習(ML)の統合は、多パラメーター性能指標に基づいた動的な最適化を可能にしています。
**2. プロセス強化と連続生産パラダイムへの移行:**
プロセス強化と連続生産パラダイムの収束は、上流開発戦略を再構築しています。業界リーダーは、強化されたバイオリアクター構成と灌流ベースの培養システムを採用しており、これらは長期間にわたって高い細胞生存率と生産性を維持できる細胞株を必要とします。これらの変化は、開発期間を短縮するだけでなく、施設全体のフットプリントと資源消費を削減し、CHO細胞株開発を持続可能なバイオ医薬品生産の主要なイネーブラーとして位置づけています。
**3. 規制要件の厳格化:**
規制当局は、細胞株特性評価の基準を引き上げており、遺伝的安定性、コピー数組込み、クローン純度に関する詳細な評価を求めています。このため、サービスプロバイダーは、厳格なコンプライアンス要件を満たす堅牢なデータセットを生成するために、次世代プラットフォームへの投資を強化しています。
**4. 米国関税の導入とサプライチェーンの再編:**
2025年に導入された主要なバイオテクノロジー試薬、細胞培養装置、重要な消耗品に対する新たな米国関税は、CHO細胞株開発サービスに連鎖的な影響を与えています。輸入関税の追加は、血清代替品、シングルユースバイオリアクターコンポーネント、分子生物学酵素などの必須品目のリードタイムを増加させ、組織はサプライヤーネットワークを再評価するよう促されました。多くの開発チームは、コスト圧力を軽減し、プロジェクトのタイムラインを中断なく維持するために、調達戦略の多様化、国内メーカーの探索、および数量ベースの契約交渉によって対応しています。これにより、コスト効率の高いプロセス設計への注目が高まり、資源利用を最適化するモジュラーワークセルやリーンな施設レイアウトへの関心が促進されています。
### 展望
CHO細胞株開発サービス市場の将来は、技術革新、戦略的パートナーシップ、および地域ごとの適応によって形成されるでしょう。
**1. セグメンテーションの多様化とニーズの細分化:**
市場は、エンドユーザー、ビジネスモデル、発現技術、アプリケーション、およびサービスタイプによって細分化されており、それぞれのセグメントで異なるニーズと意思決定基準が存在します。
* **エンドユーザー:** 学術・研究機関は柔軟性と実験の自由度を重視し、迅速なターンアラウンドとカスタマイズ可能なスクリーニングパネルを優先します。一方、バイオ医薬品企業は、後期開発および商業生産をサポートするために、堅牢でスケーラブルなワークフローと深い規制専門知識を求めます。受託研究機関(CRO)は、多様なクライアントプロジェクトに対応する技術的汎用性と、厳格なプロジェクトタイムラインを満たす運用上の堅牢性の両方を必要とします。
* **ビジネスモデル:** 自社開発グループは、長期的なコスト管理とシームレスな技術移転を重視し、開発ワークフローを広範なプロセス開発および製造ネットワークに統合します。アウトソースプロバイダーは、初期の細胞株特性評価からマスターセルバンキング、規制サポートまで、専門的なプラットフォームへのアクセスを可能にするモジュラーサービスを提供します。
* **発現技術:** 人工染色体技術に基づくプラットフォームは、複雑なコンストラクト発現のための広範なゲノム容量を提供し、非ウイルス性またはウイルス性ベクターを用いたランダム組込みアプローチは、迅速でハイスループットなスクリーニングを実現します。Cre-Lox組換え、CRISPR-Cas技術、ジンクフィンガーヌクレアーゼシステムなどの部位特異的技術は、高価値分子の要求をサポートする精度と安定性を提供します。
* **アプリケーション:** モノクローナル抗体から組換えタンパク質、ワクチンに至るまでのアプリケーションは、高容量生産性、グリコシル化の一貫性、ウイルス除去適合性など、特定の細胞株属性を必要とします。
* **サービスタイプ:** 細胞株特性評価、クローンスクリーニング、遺伝子工学、GMPまたは研究グレードでのマスターセルバンキング、および規制サポートを含むサービスタイプは、開発の包括的な性質を反映しており、科学的厳密性とコンプライアンス要件を両立させる統合ソリューションの重要性を強調しています。
**2. 地域ごとの戦略と市場の進化:**
地域ごとのダイナミクスは、CHO細胞株開発の優先順位とサービス提供モデルに大きな影響を与えます。
* **南北アメリカ:** 堅牢な研究エコシステムと多額のバイオ医薬品投資が、自動化、ハイスループットスクリーニング、高度な分析を統合したターンキーソリューションへの需要を促進しています。確立された規制経路と深い資本市場が、新しい発現プラットフォームとデジタル追跡システムの迅速な採用を促進しています。
* **EMEA(ヨーロッパ、中東、アフリカ):** 規制体制と市場成熟度が多様であり、集中的な欧州ガイドラインと国レベルの承認プロセスの違いが共存しています。この地域のプロバイダーは、多様なコンプライアンス環境を乗り切るために、品質システムのローカライズと学術機関との戦略的提携を重視しています。
* **アジア太平洋:** 中国とインドの大規模な製造拠点は、国内および世界の需要をサポートするために上流の生産能力を拡大しています。主要市場の規制当局は、バイオセーフティと細胞バンクの認定基準を強化しており、サービスプロバイダーは包括的なマスターセルバンキングと遺伝的安定性試験を含むサービス提供を拡大しています。
**3. 主要組織の戦略と協力:**
主要な組織は、戦略的投資と先駆的な研究協力を組み合わせることで、CHO細胞株開発サービスにおいて新たなベンチマークを設定しています。主要なライフサイエンスサプライヤーは、専門サービスプロバイダーや独自の技術プラットフォームの買収を通じて事業を拡大し、ハイスループットクローンスクリーニングから高度な遺伝子編集に至るまでの能力を統合しています。受託研究機関は、エンゲージメント範囲と技術サポートの深さにおいて柔軟性を提供するモジュラーサービスモデルを通じて差別化を図っています。自動化された細胞培養ワークステーションとクラウドベースのデータ管理システムへの投資により、これらのプロバイダーは透明性を高め、細胞株性能指標のリアルタイム監視を可能にしています。設備ベンダー、試薬サプライヤー、エンドユーザー間の協力ネットワークはますます一般的になり、標準化されたスケーラブルなワークフローを提供する統合エコシステムへの傾向を反映しています。知的財産戦略とクロスライセンス契約は、部位特異的組込み技術への広範なアクセスを促進し、共有された検証プロトコルは、複数の管轄区域にわたるコンプライアンスを合理化しています。
**4. 業界リーダーのための戦略的示唆:**
CHO細胞株開発サービス業務を最適化するために、組織は精密遺伝子編集プラットフォームの採用を優先し、一貫したクローン挙動を確保し、下流のプロセス移転を合理化するために部位特異的組込み技術に焦点を当てるべきです。ハイスループットスクリーニングの自動化とAI駆動型分析への投資は、意思決定の精度を高め、開発期間を短縮し、高性能候補の迅速な特定を可能にします。サプライチェーンのレジリエンスは、多様な調達戦略と試薬および設備サプライヤーとの戦略的パートナーシップを通じて対処されるべきです。国内および地域での供給契約を確立することは、国際関税や物流の混乱の影響を軽減し、共同での処方開発は単一供給源材料への依存を減らします。リスク評価には地政学的要因を組み込み、調達、品質、法務チームが連携してプロジェクトの継続性を維持する必要があります。規制との整合性は極めて重要であり、検証およびコンプライアンスの専門家との早期の連携は、特性評価要件を開発ワークフローに統合し、技術移転および臨床段階移行中の遅延を削減します。組織は、品質設計(Quality-by-Design)原則を組み込み、データ豊富なプラットフォームを活用して、グローバルな規制基準を満たす堅牢な証拠パッケージを生成することが奨励されます。最後に、学術センターや技術革新者との提携を通じて協力的な研究エコシステムを育成することは、新たな発現技術へのアクセスを加速し、細胞株性能の持続的な改善を推進するでしょう。
これらの戦略的洞察は、CHO細胞株開発サービス市場の進化する環境をナビゲートし、加速された開発タイムライン、最適化された資源配分、および持続的な競争優位性を実現するための道筋を示しています。
以下に、ご指定の「CHO細胞株開発サービス」を正確に使用し、詳細な階層構造で目次を日本語に翻訳します。
—
**目次**
* **序文**
* 市場セグメンテーションと対象範囲
* 調査対象期間
* 通貨
* 言語
* ステークホルダー
* **調査方法**
* **エグゼクティブサマリー**
* **市場概要**
* **市場インサイト**
* CHO細胞株最適化ワークフローを加速するためのCRISPR Cas9および塩基編集技術の採用
* 開発初期段階で高生産性CHOクローンを特定するためのシングルセルRNAシーケンシングプラットフォームの統合
* CHO細胞培養プロセスにおける培地および飼料最適化のためのAI駆動型予測モデリングの利用増加
* CHO細胞株の安定性と収量を向上させる次世代合成プロモーターの開発
* CHO培養の生産性と一貫性を向上させるための連続灌流バイオリアクターシステムの導入
* 特注のCHO細胞株開発プロジェクトにおけるバイオテクノロジー企業とCDMO間のアウトソーシングパートナーシップの拡大
* **2025年の米国関税の累積的影響**
* **2025年の人工知能の累積的影響**
* **CHO細胞株開発サービス市場、サービスタイプ別**
* 細胞株特性評価
* クローン選別
* 遺伝子工学
* マスターセルバンキング
* GMPグレード
* 研究グレード
* 規制サポート
* **CHO細胞株開発サービス市場、発現技術別**
* 人工染色体技術
* ランダム組込み
* 非ウイルスベクター
* ウイルスベクター
* 部位特異的組込み
* Cre-Lox組換え
* CRISPR-Cas技術
* ジンクフィンガーヌクレアーゼ
* **CHO細胞株開発サービス市場、ビジネスモデル別**
* インハウス
* アウトソース
* **CHO細胞株開発サービス市場、エンドユーザー別**
* 学術・研究機関
* バイオ医薬品企業
* 受託研究機関 (CRO)
* **CHO細胞株開発サービス市場、用途別**
* モノクローナル抗体
* 組換えタンパク質
* ワクチン
* **CHO細胞株開発サービス市場、地域別**
* 米州
* 北米
* 中南米
* 欧州、中東、アフリカ
* 欧州
* 中東
* アフリカ
* アジア太平洋
* **CHO細胞株開発サービス市場、グループ別**
* ASEAN
* GCC
* 欧州連合
* BRICS
* G7
* NATO
* **CHO細胞株開発サービス市場、国別**
* 米国
* カナダ
* メキシコ
* ブラジル
* 英国
* ドイツ
* フランス
* ロシア
* イタリア
* スペイン
* 中国
* インド
* 日本
* オーストラリア
* 韓国
* **競争環境**
* 市場シェア分析、2024年
* FPNVポジショニングマトリックス、2024年
* 競合分析
* AGCバイオロジクス
* アラジェン・ライフサイエンス
* メルクKGaA
* ベーリンガーインゲルハイム・インターナショナルGmbH
* BPSバイオサイエンス社
* カタレント社
* チャールズ・リバー・ラボラトリーズ
* クリエイティブ・バイオアレイ
* キュリア
* ユーロフィン・サイエンティフィックS.E.
* エクセルジーンSA
* フェアジャーニー・バイオロジクス
* 富士フイルム・ダイオシンス・バイオテクノロジーズ
* ジェンスクリプト・バイオテック・コーポレーション
* GTPバイオウェイズ
* ホライゾン・ディスカバリー
* KBIバイオファーマ
* ロンザ・グループLtd
* サムスン・バイオロジクスCo Ltd
* サルトリウス・グループ
* セレクシスSA
* サーモフィッシャーサイエンティフィック社
* 薬明生物 (WuXi Biologics)
* **図目次** [合計: 30]
* 1. 世界のCHO細胞株開発サービス市場規模、2018-2032年(百万米ドル)
* 2. 世界のCHO細胞株開発サービス市場規模、サービスタイプ別、2024年対2032年(%)
* 3. 世界のCHO細胞株開発サービス市場規模、サービスタイプ別、2024年対2025年対2032年(百万米ドル)
* 4. 世界のCHO細胞株開発サービス市場規模、発現技術別、2024年対2032年(%)
* 5. 世界のCHO細胞株開発サービス市場規模、発現技術別、2024年対2025年対2032年(百万米ドル)
* 6. 世界のCHO細胞株開発サービス市場規模、ビジネスモデル別、2024年対2032年(%)
* 7. 世界のCHO細胞株開発サービス市場規模、ビジネスモデル別、2024年対2025年対2032年(百万米ドル)
* 8. 世界のCHO細胞株開発サービス市場規模、エンドユーザー別、2024年対2032年(%)
* 9. 世界のCHO細胞株開発サービス市場規模、エンドユーザー別、2024年対2025年対2032年(百万米ドル)
* 10. 世界のCHO細胞株開発サービス市場規模、用途別、2024年対2032年(%)
* 11. 世界のCHO細胞株開発サービス市場規模、用途別、2024年対2025年対2032年(百万米ドル)
* 12. 世界のCHO細胞株開発サービス市場規模、地域別、2024年対2025年対2032年(百万米ドル)
* 13. 米州のCHO細胞株開発サービス市場規模、サブ地域別、2024年対2025年対2032年(百万米ドル)
* 14. 北米のCHO細胞株開発サービス市場規模、国別、2024年対2025年対2032年(百万米ドル)
* 15. 中南米のCHO細胞株開発サービス市場規模、国別、2024年対2025年対2032年(百万米ドル)
* 16. 欧州、中東、アフリカのCHO細胞株開発サービス市場規模、サブ地域別、2024年対2025年対2032年(百万米ドル)
* 17. 欧州のCHO細胞株開発サービス市場規模、国別、2024年対2025年対2032年(百万米ドル)
* 18. 中東のCHO細胞株開発サービス市場規模、国別、2024年対2025年対2032年(百万米ドル)
* 19. アフリカのCHO細胞株開発サービス市場規模、国別、2024年対2025年対2032年(百万米ドル)
* 20. アジア太平洋のCHO細胞株開発サービス市場規模、国別、2024年対2025年対2032年(百万米ドル)
* 21. 世界のCHO細胞株開発サービス市場規模、グループ別、2024年対2025年対2032年
* **表目次** [合計: 657]
*** 本調査レポートに関するお問い合わせ ***

CHO細胞は、組換えタンパク質を生産する宿主細胞として、今日のバイオ医薬品産業において中核を成す存在です。特に、抗体医薬や遺伝子治療薬といった高機能性医薬品の製造には不可欠であり、その安定した供給は世界中の患者の健康に直結しています。このような背景のもと、「CHO細胞株開発サービス」は、医薬品開発企業が効率的かつ高品質な細胞株を確立するための専門的な支援を提供するものであり、バイオ医薬品市場の急速な拡大に伴い、その需要と重要性は飛躍的に高まっています。このサービスは、単なる技術提供に留まらず、開発期間の短縮、コストの最適化、そして最終製品の品質保証に貢献する戦略的なパートナーシップとしての価値を持っています。
CHO細胞がバイオ医薬品生産の主要なプラットフォームとして選ばれる理由は多岐にわたり、その優位性は揺るぎないものです。まず、ヒト細胞に近い翻訳後修飾、特に複雑な糖鎖修飾を行う能力が高く、これにより医薬品としての有効性、安定性、そして安全性が確保されます。また、高い増殖能力と培養適応性、そして大規模培養における安定したタンパク質発現能力も大きな利点です。さらに、長年にわたる使用実績から、米国食品医薬品局(FDA)をはじめとする各国の規制当局からの承認実績が豊富であり、安全性に関する懸念が少ない点も、医薬品開発において極めて重要な要素となっています。これらの特性が、CHO細胞をバイオ医薬品製造における事実上の標準たらしめているのです。
CHO細胞株開発サービスが提供するプロセスは、多段階にわたる高度な専門技術の集積です。初期段階では、目的とする治療用タンパク質の遺伝子をCHO細胞に導入するための発現ベクターの設計と構築が行われます。このベクターは、高効率な遺伝子導入と安定したタンパク質発現を可能にするよう最適化されます。次に、遺伝子が導入された多数の細胞の中から、目的タンパク質を最も高効率かつ安定的に発現する細胞クローンを選別する作業が続きます。このクローン選別には、ハイスループットスクリーニング技術やシングルセルクローニング技術が用いられ、数千から数万に及ぶ候補の中から、わずか数個の有望な細胞株を特定します。この厳密な選別プロセスこそが、最終的な医薬品の品質と生産性を左右する鍵となります。
選定された細胞株は、さらに詳細な評価と最適化の段階へと進みます。培養条件の最適化では、細胞の増殖速度、生存率、そして目的タンパク質の発現量を最大化するための培地組成、温度、pH、溶存酸素濃度などのパラメータが綿密に検討されます。また、バイオリアクターを用いたスケールアップを見据えたプロセス開発も不可欠であり、生産性の向上と品質の均一性を両立させるための戦略が練られます。この段階では、目的タンパク質の物理化学的特性、生物学的活性、糖鎖プロファイルなどの品質特性を詳細に分析する高度な分析技術が駆使され、医薬品としての品質基準を満たしているかどうかが厳しく評価されます。これらの工程を通じて、研究室レベルの細胞株が、商業生産に耐えうる堅牢な生産システムへと昇華されていくのです。
外部のCHO細胞株開発サービスを利用する利点は計り知れません。最も顕著なのは、自社では保有が難しい最先端の設備、専門的な知識、そして長年の経験を持つエキスパートチームにアクセスできる点です。これにより、開発期間の大幅な短縮と、それに伴う市場投入までの時間の短縮が実現されます。また、初期投資やランニングコストの削減にも繋がり、特にリソースが限られるバイオベンチャー企業にとっては大きなメリットとなります。さらに、開発プロセスにおける技術的なリスクや規制対応のリスクを軽減し、顧客企業が自身のコア研究開発に集中できる環境を提供します。これらのサービスは、単に技術的な課題を解決するだけでなく、バイオ医薬品開発全体の戦略的な加速を可能にするものです。
しかしながら、CHO細胞株開発には依然として複雑な課題が存在します。例えば、超高発現株の確立、長期培養における細胞株の安定性維持、そして複雑な翻訳後修飾の精密な制御は、常に技術革新が求められる領域です。特に、バイオ医薬品の多様化に伴い、より複雑な構造を持つタンパク質や、特定の糖鎖パターンを要求される医薬品の開発が増加しており、これに対応するための細胞株エンジニアリング技術の進化が不可欠となっています。今後の展望としては、人工知能(AI)や機械学習を活用したハイスループットスクリーニングのさらなる効率化、CRISPR/Cas9などのゲノム編集技術を用いた細胞株の設計、そして連続生産システムとの統合による生産性の飛躍的な向上などが期待されています。これらの技術革新は、CHO細胞株開発の未来を形作り、より高品質で安価なバイオ医薬品の安定供給に貢献するでしょう。
結論として、CHO細胞株開発サービスは、現代のバイオ医薬品産業において、その発展と持続可能性を支える極めて重要なインフラであり、その役割は今後も拡大の一途を辿るでしょう。高度な専門知識と技術を結集し、医薬品開発の初期段階から商業生産に至るまでを一貫してサポートすることで、革新的なバイオ医薬品の創出を加速し、世界中の患者に希望をもたらす未来の医療を切り拓くことに貢献しています。