世界の脱パイロジェン無菌空バイアル市場:製品タイプ別(ガラスバイアル、プラスチックバイアル)、容量別(10 mL超、2~5 mL、5~10 mL)、滅菌方法別、用途別、エンドユーザー別 – グローバル予測 2025年~2032年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
## 脱パイロジェン無菌空バイアル市場:詳細な分析と展望
### 市場概要
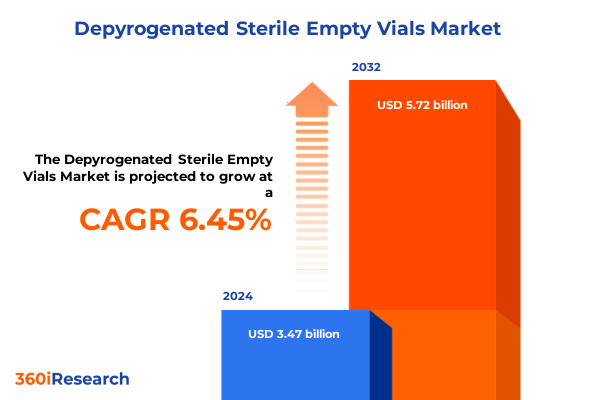
脱パイロジェン無菌空バイアル市場は、2024年に34.7億米ドルと推定され、2025年には36.8億米ドルに達すると予測されています。その後、年平均成長率(CAGR)6.45%で成長し、2032年には57.2億米ドル規模に達する見込みです。この市場は、現代の急速に進化するヘルスケア環境において、生物学的製剤、高度な診断薬、ワクチン開発など、多岐にわたる重要なアプリケーションの基盤となる構成要素として不可欠な役割を担っています。これらのバイアルは、高感度な製剤の安全な封じ込めと投与を保証し、厳格な無菌性およびパイロジェンフリー性能の要件を満たすことで、製薬メーカー、研究機関、臨床検査機関にとって不可欠な存在となっています。
世界中の規制当局は、容器の完全性に関するガイドラインを強化しており、妥協の余地はありません。これにより、業界関係者は、コンプライアンス要件を先取りし、患者の転帰を保護するために、材料選択、滅菌プロセス、品質保証プロトコルに関する包括的な理解を維持することが求められています。サプライチェーンの混乱や需要パターンの変化といった課題に直面する中、脱パイロジェン無菌空バイアルの戦略的役割は過小評価できません。製造能力、原材料調達、および新たなイノベーションに対する明確な洞察は、意思決定者が業務を最適化し、強靭な供給ネットワークを育成するために不可欠です。
### 市場を牽引する要因
脱パイロジェン無菌空バイアル市場は、技術革新、規制の進展、および多様な市場要因によって大きく変革されています。
**1. 技術革新と材料科学の進歩:**
バイアル充填の自動化、高度な脱パイロジェン技術、およびデジタルシリアル化システムは、製造パラダイムを急速に再定義しています。これらの革新は、スループットと精度を向上させるだけでなく、サプライチェーンの監視が強化される時代において不可欠なリアルタイムのトレーサビリティを可能にします。同時に、材料科学のブレークスルーは次世代バイアルへの道を開いています。従来のガラスバイアルに加え、ポリエチレンやポリプロピレンなどの高品位プラスチックが、破損耐性や軽量化の利点を提供し、注目を集めています。ガラス組成も進化しており、特殊な琥珀色製剤は、光に敏感な生物学的製剤に対して優れた保護を提供します。その結果、容器のカスタマイズがサプライヤー間の競争上の差別化要因として浮上しています。さらに、化学的不活性と耐久性を向上させる独自のガラスコーティングや、両素材の最良の特性を提供するように設計されたハイブリッドプラスチック-ガラス複合材への投資も進んでいます。
**2. 規制の強化とコンプライアンス要件:**
規制当局は、容器閉鎖の完全性とパイロジェン除去に関する基準を引き続き引き上げており、関係者により厳格な検証プロトコルの採用を促しています。より厳格なガイドラインと急速に進化するエンドユーザーの要件の融合は、バイアルメーカーとサービスプロバイダー間の戦略的提携を強化しています。企業は、将来を見据えたアプローチを採用することで、コンプライアンスの課題を乗り越え、運用効率を向上させ、医学的に影響力のある次世代治療法をサポートする立場にあります。
**3. 注射療法の普及と新たな治療法の台頭:**
細胞・遺伝子治療、mRNAベースのワクチンにおけるブレークスルーによって推進される注射療法の増加は、信頼性の高いバイアル供給チェーンの重要性を強調しています。特に、COVID-19およびインフルエンザプラットフォームに焦点を当てたワクチン製造業者は、大規模な予防接種キャンペーンを合理化するために、大容量かつバッチ追跡可能なソリューションを求めています。
**4. 米国関税の影響とサプライチェーンの再構築:**
2025年に米国政府が導入した、滅菌バイアル製造に不可欠な主要原材料および生産設備を対象とした関税は、当初、輸入部品に依存する多くのバイアル生産者にとって投入コストの上昇をもたらしました。しかし、この措置は、国内生産能力を強化することを目的としており、価格圧力が高まるにつれて、多くの組織は現地生産施設への投資を加速させたり、より安定したコスト構造を確保するために長期的なサプライヤーパートナーシップを構築したりしました。戦略的な在庫管理が優先事項となり、企業はさらなる関税変動や潜在的な混乱に備えて安全在庫レベルを調整しました。これにより、国内のガラスおよび樹脂サプライヤーは能力を増強し、受託製造業者は社内滅菌および包装を含むサービス提供を多様化させ、最終的にサプライチェーンの回復力強化に貢献しました。
**5. エンドユーザーおよびアプリケーションの多様なニーズ:**
製品タイプ、アプリケーション、エンドユーザー、容量、および滅菌方法によるセグメンテーションの微妙な理解は、市場の明確なダイナミクスを明らかにします。
* **製品タイプ:** ガラス製バイアルでは、光に敏感な生物学的製剤には琥珀色製剤が好まれ、一般的な注射用途には透明ガラスが標準です。ポリエチレン製バイアルは耐久性と破損リスクの低さで評価され、ポリプロピレン製オプションは優れた耐薬品性を提供し、診断試薬に対応します。
* **アプリケーション:** 細胞・遺伝子治療プロセスは超精密なバイアル仕様を要求し、メーカーはより厳密な公差と厳格な脱パイロジェン検証を提供する必要があります。臨床化学では、高容量のワークフローは標準化された閉鎖システムを備えた透明な容器に依存し、免疫診断および分子診断では自動分析装置と互換性のあるバイアルが優先されます。
* **エンドユーザー:** バイオテクノロジー企業は通常、独自の製剤をサポートするために特注のバイアル設計で協力します。病院ベースおよび独立した診断ラボは、一貫した供給と迅速なターンアラウンドを必要とし、地域に特化した在庫戦略を推進します。ジェネリックメーカーは、費用対効果が高く、かつ品質に準拠したプラスチック代替品を評価することがよくあります。
* **容量:** 分子アッセイには2mLまでの小容量バイアルが好まれ、バルク充填作業には10mLを超える大容量フォーマットが広く使用されます。
* **滅菌方法:** オートクレーブプロセスはガラス容器に広く普及しており、エチレンオキシドは熱に敏感なプラスチックに人気があり、ガンマ線照射は迅速なスループットと堅牢な微生物不活化のためにますます採用されています。
**6. 地域別成長要因:**
* **米州:** 成熟したバイオ医薬品エコシステムと堅牢な国内製造能力の融合により、脱パイロジェン無菌空バイアルに対する安定した需要環境が育まれています。北米の生産者は、高度な材料専門知識と合理化された規制経路を活用しており、ラテンアメリカ市場は、地域のヘルスケアイニシアチブが予防接種と診断検査の取り組みを強化するにつれて、拡大の初期兆候を示しています。
* **欧州、中東、アフリカ:** この地域は、多様な規制体制と主要サプライヤー間の統合によって特徴付けられます。西ヨーロッパの関係者は、統合された供給ネットワークと確立された品質フレームワークの恩恵を受けていますが、中東およびアフリカの新興市場は、受託製造および地域に特化した滅菌サービスの機会を推進しています。
* **アジア太平洋:** 中国、インド、東南アジアのバイオテッククラスターへの投資の拡大に牽引され、最も急速な変革率を示しています。政府の奨励策と国内および輸出市場の両方からの需要の増加により、地元のバイアル生産者は能力を急速に強化しています。多国籍企業と地元企業の両方が材料革新と国際基準への準拠に焦点を強化するにつれて、競争力のある価格構造と上昇する品質ベンチマークが共存しています。
**7. 戦略的投資と業界連携:**
脱パイロジェン無菌空バイアル分野の主要メーカーは、戦略的な資本配分と異業種間のコラボレーションを通じて成長経路を築いています。生産能力の拡大と自動化に資源を投入することで、厳格な品質管理を維持しながらスループットを向上させています。滅菌サービスプロバイダーや容器閉鎖システム専門家とのパートナーシップは、彼らの価値提案をさらに強化します。イノベーションパイプラインは焦点となっており、いくつかの企業は化学的不活性と耐久性を向上させる独自のガラスコーティングに投資しています。バイオ医薬品開発企業や診断機器メーカーとの共同事業は、エンドツーエンドのソリューション提供の重要性を強調しています。共同開発契約を通じて、バイアルサプライヤーは新たな製剤要件に関する重要な洞察を得て、プロセスを洗練し、検証タイムラインを加速させることができます。並行して、持続可能性が企業の課題として浮上しており、リサイクルコンテンツ、廃棄物最小化プログラム、および低炭素製造フットプリントへの投資を促しています。
### 市場の展望
脱パイロジェン無菌空バイアル市場は、2032年までに57.2億米ドルに達するという予測が示すように、今後も持続的な成長が見込まれます。業界のダイナミクスが変化し続ける中、企業は予期せぬ混乱に対してサプライチェーンを強化するために、将来を見据えた戦略を採用する必要があります。
**1. サプライチェーンの回復力強化:**
ガラス、樹脂、滅菌装置の調達チャネルを多様化することは、地政学的または経済的要因が変動をもたらす際に、生産の継続性を維持するのに役立ちます。複数のティアワンサプライヤーとの関係を強化することは、集中リスクをさらに軽減します。リアルタイムの在庫追跡、重要機器の予測保守、需要変動を予測するための高度な分析などのデジタルツールを統合することで、運用上の俊敏性を高めることができます。データ駆動型の洞察を活用することで、組織はバッチスケジューリングを最適化し、リードタイムを短縮し、全体的な資源利用を改善できます。製造ワークフロー全体に品質設計(QbD)原則を組み込むことは、堅牢なコンプライアンスを確保し、規制当局への申請を迅速化します。
**2. 継続的なイノベーションと共同開発:**
新たな市場セグメントを活用するために、企業はバイオテックおよび診断企業との共同イノベーションパートナーシップを検討すべきです。製品開発サイクルの初期段階で関与することで、容器仕様、滅菌要件、および充填プロセスに関する整合が可能になります。また、エネルギー効率の高い滅菌ラインからリサイクル可能な材料イニシアチブに至るまで、持続可能な製造慣行への投資は、進化するESG(環境・社会・ガバナンス)の期待に応え、ブランドの評判を強化します。
**3. 規制遵守と競争優位性の維持:**
規制当局および業界団体との積極的な対話を維持することは、進化する基準に関する高度な可視性を提供します。政策変更を予測する組織は、最小限の運用上の摩擦で検証プロトコルと認証戦略を再調整でき、継続的な改善を促進し、競争上の優位性を確保します。競争が激化するにつれて、運用上の卓越性、製品革新、および戦略的提携を組み合わせる能力が市場リーダーを際立たせるでしょう。進化する顧客の期待と規制要件にビジネスモデルを合わせる関係者は、競争上の優位性を強化し、長期的な回復力を育むことができます。
以下に、ご指定のTOCの日本語訳と詳細な階層構造を示します。
—
**目次**
* **序文**
* 市場セグメンテーションとカバレッジ
* 調査対象年
* 通貨
* 言語
* ステークホルダー
* **調査方法**
* **エグゼクティブサマリー**
* **市場概要**
* **市場インサイト**
* 生物学的製剤送達のための使い捨て脱パイロジェン無菌空ガラスバイアルの採用増加
* エンドトキシン試験認証付き脱パイロジェン無菌空バイアルの需要を促進する規制強化
* 個別化医療および希少疾患治療をサポートするための脱パイロジェン無菌空バイアルのカスタマイズへの移行
* 空バイアル製造における無菌保証を強化するための高度な脱パイロジェン技術の統合
* 世界的なワクチン展開とパンデミック対策の中での脱パイロジェン無菌空バイアル生産能力の拡大
* 臨床試験におけるターンキー脱パイロジェンサービスのためのバイアルメーカーと製薬会社間の提携拡大
* **2025年米国関税の累積的影響**
* **2025年人工知能の累積的影響**
* **脱パイロジェン無菌空バイアル市場、製品タイプ別**
………… (以下省略)
*** 本調査レポートに関するお問い合わせ ***

「脱パイロジェン無菌空バイアル」は、現代の医薬品、バイオテクノロジー、診断薬分野で、安全性と有効性を担保する不可欠な容器である。その名称は、パイロジェンが除去され無菌であり、内容物が充填されていない小型容器であることを示す。特に注射剤やワクチンなど、直接人体に投与される製剤の容器として用いられるため、その品質には極めて高い基準が求められる。これらのバイアルは、単なる入れ物ではなく、最終製品の品質を決定づける重要な要素であり、患者の健康と安全を直接的に左右する役割を担っている。
「無菌」であることは、バイアル内に生存可能な微生物が一切存在しない状態を指す。これは、充填される薬剤が微生物によって汚染され、患者に感染症やその他の有害事象を引き起こすリスクを排除するために絶対的に必要である。無菌状態達成には、高圧蒸気滅菌、乾熱滅菌、ガンマ線照射、または無菌操作法などが用いられる。特に、注射剤のように体内に直接導入される製剤の場合、微生物汚染は敗血症などの重篤な健康被害に直結するため、バイアルの無菌性は医薬品製造における最優先事項の一つとして厳格に管理されている。
一方、「脱パイロジェン」は、バイアルからパイロジェン、特にグラム陰性菌の細胞壁由来であるエンドトキシンを除去することを意味する。パイロジェンは、たとえ微生物自体が死滅していても、その残骸が発熱、悪寒、血圧低下、さらにはショック症状といった重篤な生理的反応を引き起こす可能性があるため、無菌性とは別に除去が必須となる。脱パイロジェン化は、通常、高温での乾熱処理(250℃以上で30分以上など)によって行われ、エンドトキシンを分解・不活性化させる。その除去確認には、カブトガニの血球抽出液を用いるリムルス試薬(LAL)試験が広く用いられ、極微量のパイロジェンも高感度に検出される。無菌性と脱パイロジェン性は、共に患者の安全を確保するための二本柱であり、どちらか一方が欠けても医薬品としての品質は保証されない。
高性能バイアルの製造プロセスは、極めて厳格な品質管理の下で行われる。原材料のガラスは、化学的安定性に優れ、薬剤との相互作用が少ないホウケイ酸ガラスが主に選定される。製造は、微粒子や微生物の混入を徹底的に防ぐため、クリーンルームと呼ばれる清浄度の高い環境で行われ、洗浄、乾燥、滅菌、脱パイロジェン化の各工程が厳密に管理される。さらに、バイアルの寸法精度、表面の欠陥、異物の有無、そしてもちろん無菌性やパイロジェンレベルの検査など、多岐にわたる品質試験が実施される。これらの工程は、医薬品の製造管理および品質管理基準であるGMP(Good Manufacturing Practice)に準拠し、製品の一貫性と信頼性を保証する上で不可欠である。
脱パイロジェン無菌空バイアルは、その厳格な品質基準ゆえに、生命科学分野における多種多様な用途で不可欠な存在となっている。具体的には、点滴剤、注射用抗生物質、インスリン、ワクチン、血液製剤、遺伝子治療薬といった医薬品のほか、細胞培養用培地、診断薬、研究用試薬の保存容器としても広く利用されている。これらのバイアルが提供する安全性と信頼性は、最終的に患者への安全な医療提供を可能にし、医薬品開発の進展を支える基盤となっている。今後も、より高度な品質要求や環境負荷低減への対応など、その進化は止まることなく、医療と科学の発展に貢献し続けるであろう。