世界のバイオプロセスバリデーション市場:コンポーネント別(サービス、ソフトウェア、バリデーション機器・消耗品)、バリデーションタイプ別(洗浄バリデーション、機器バリデーション、プロセスバリデーション)、バイオ医薬品タイプ、プロセスコンポーネント、ワークフロー段階、スケール、モード、エンドユーザー別 – グローバル予測 2025年-2030年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
「バイオプロセスバリデーション市場:2025-2030年グローバル予測」と題された360iResearchの最新レポートは、バイオ医薬品製造における品質、安全性、および規制遵守を保証する上で不可欠な**バイオプロセスバリデーション**の世界市場に関する包括的な分析を提供しています。2025年12月に発行されたこのレポートは、市場の現状、主要な推進要因、そして将来の成長機会について詳細な洞察を提供しています。市場は2024年に4億8587万米ドル、2025年には5億3767万米ドルに達すると予測されており、2025年から2030年にかけて年平均成長率(CAGR)10.98%で成長し、2030年には9億796万米ドルに達すると見込まれています。この堅調な成長は、バイオ医薬品産業の拡大と、それに伴う厳格な規制要件への対応の必要性によって牽引されています。
**市場概要(Market Overview)**
**バイオプロセスバリデーション**は、バイオ医薬品の製造プロセスが意図した結果を一貫して達成できることを科学的に証明し、文書化する一連の活動を指します。これには、原材料の受け入れから最終製品の放出に至るまでの全工程において、機器、プロセス、洗浄手順、分析方法などが適切に機能していることを検証する作業が含まれます。市場は、サービス、ソフトウェア、バリデーション機器・消耗品といった主要なコンポーネントに分類されます。サービスセグメントは、専門的なコンサルティング、試験、監査サービスを含み、特に複雑なバイオプロセスや新規モダリティに対応するために不可欠です。ソフトウェアセグメントは、データ管理、分析、文書化、および規制遵守を支援するデジタルソリューションを提供し、効率性とトレーサビリティを向上させます。バリデーション機器・消耗品セグメントは、プロセス監視、品質管理、および試験に必要な物理的ツールと材料を供給します。
バリデーションの種類としては、洗浄バリデーション、機器バリデーション、プロセスバリデーションが挙げられます。洗浄バリデーションは、製造装置が次のバッチ生産前に適切に洗浄され、汚染がないことを保証します。機器バリデーションは、製造および試験に使用されるすべての機器が正確かつ一貫して機能することを確認します。プロセスバリデーションは、製造プロセス全体が安定しており、常に高品質の製品を生産できることを実証します。これらのバリデーション活動は、バイオ医薬品の品質、安全性、有効性を確保し、患者の健康を守る上で極めて重要です。
さらに、レポートでは、バイオロジックの種類(モノクローナル抗体、ワクチン、遺伝子・細胞治療など)、プロセスコンポーネント、ワークフロー段階、スケール(臨床前、臨床、商業生産)、モード(インハウス、アウトソース)、およびエンドユーザー(バイオ医薬品メーカー、CDMO/CRO、学術・研究機関など)といった多様なセグメンテーションに基づいて市場を分析しています。グローバル市場としての性質上、各地域の規制要件や産業構造の違いが市場の動向に影響を与えますが、全体としては、バイオ医薬品の複雑化と製造プロセスの高度化に伴い、より包括的で専門的な**バイオプロセスバリデーション**ソリューションへの需要が高まっています。特に、細胞・遺伝子治療のような革新的な治療法の登場は、従来のバリデーション手法では対応しきれない新たな課題を提示しており、これに対応するための新しい技術やアプローチの開発が急務となっています。
**市場の推進要因(Drivers)**
**バイオプロセスバリデーション**市場の成長を推進する主要な要因は多岐にわたります。最も顕著な要因の一つは、世界的な規制環境の厳格化です。米国食品医薬品局(FDA)、欧州医薬品庁(EMA)、日本の医薬品医療機器総合機構(PMDA)をはじめとする各国の規制当局は、バイオ医薬品の安全性と有効性に関する基準を継続的に引き上げています。これにより、製薬企業は、製造プロセスのあらゆる段階で厳格なバリデーションを実施し、その結果を詳細に文書化することが義務付けられています。規制遵守は、市場参入、製品承認、および市場での競争力を維持するために不可欠であり、**バイオプロセスバリデーション**への投資を促進しています。
次に、バイオ医薬品市場自体の急速な成長が挙げられます。モノクローナル抗体、組換えタンパク質、ワクチン、そして近年注目を集める遺伝子治療や細胞治療といった革新的なバイオ医薬品の開発と商業化が活発化しています。これらの製品は、従来の低分子医薬品と比較して分子構造が複雑であり、製造プロセスも高度な技術と厳密な管理を必要とします。そのため、製造プロセスの堅牢性と再現性を保証するための**バイオプロセスバリデーション**の重要性が増しています。特に、個別化医療の進展に伴い、小規模バッチ生産や迅速な製造が求められるケースが増えており、これに対応するための柔軟かつ効率的なバリデーション手法が求められています。
技術革新もまた、市場の重要な推進要因です。リアルタイムプロセス分析(PAT)、自動化システム、高度なデータ解析ツール、そして人工知能(AI)や機械学習(ML)の導入により、**バイオプロセスバリデーション**の精度、効率、およびコスト効率が向上しています。これらの技術は、プロセスの変動を早期に検出し、リスクを軽減し、より迅速な意思決定を可能にします。例えば、インラインセンサーやオンラインモニタリングシステムは、製造中に重要なプロセスパラメーターを継続的に監視し、リアルタイムでのバリデーションデータ収集を可能にすることで、最終製品の品質保証を強化します。
さらに、バイオ医薬品企業による製造およびバリデーション業務のアウトソーシングの増加も市場を牽引しています。多くのバイオ医薬品企業、特に中小規模のバイオテクノロジー企業は、自社で全ての製造施設やバリデーション専門知識を保有することが困難であるため、契約製造受託機関(CDMO)や契約研究受託機関(CRO)にこれらの業務を委託しています。CDMO/CROは、専門的な知識、経験、および設備を提供することで、効率的かつ規制に準拠した**バイオプロセスバリデーション**サービスを提供し、市場の成長に貢献しています。
最後に、製品の品質と患者の安全性に対する絶え間ない要求も、**バイオプロセスバリデーション**の需要を押し上げています。医薬品の品質不良は、患者の健康に深刻な影響を与えるだけでなく、企業の評判失墜、リコール、および巨額の経済的損失につながる可能性があります。したがって、製造プロセスの初期段階から厳格なバリデーションを実施することで、これらのリスクを最小限に抑え、高品質で安全なバイオ医薬品を安定的に供給することが、業界全体の最優先事項となっています。
**市場の展望(Outlook)**
**バイオプロセスバリデーション**市場は、予測期間である2025年から2030年にかけて、年平均成長率10.98%という堅調なペースで成長を続けると予測されており、その将来性は非常に明るいと言えます。この成長は、前述の推進要因が引き続き市場に影響を与えることに加え、いくつかの新たなトレンドによってさらに加速されるでしょう。
まず、技術統合の深化が市場の将来を形作る重要な要素となります。AI、機械学習、ビッグデータ解析といった先進技術は、**バイオプロセスバリデーション**の領域において、予測モデリング、リスク評価、プロセス最適化、およびリアルタイムモニタリングの能力を飛躍的に向上させます。これにより、バリデーションプロセスはより効率的かつデータ駆動型になり、潜在的な問題を未然に防ぎ、製造の堅牢性を高めることが可能になります。デジタルツイン技術の導入も期待されており、物理的な製造プロセスを仮想空間でシミュレートすることで、バリデーションの計画と実行を最適化する道が開かれるでしょう。
次に、グローバルな規制環境の進化と標準化への動きが挙げられます。各国・地域で異なる規制要件が存在する現状に対し、国際的なハーモナイゼーションの努力が続けられています。これにより、**バイオプロセスバリデーション**の実施における一貫性が高まり、グローバルな製品展開が容易になる可能性があります。また、細胞・遺伝子治療製品のような新規モダリティに特化したバリデーションガイドラインの策定が進むことで、これらの革新的な治療法の開発と商業化がさらに加速されるでしょう。
さらに、個別化医療や少量生産の増加に伴い、より柔軟で適応性の高い**バイオプロセスバリデーション**ソリューションへの需要が高まります。従来のバッチ生産モデルに最適化されたバリデーション手法に加え、連続生産やモジュール式製造システムに対応した新しいアプローチが開発されることが予想されます。これにより、迅速な製品開発と市場投入が可能となり、患者へのアクセスが改善されることが期待されます。
市場セグメント別に見ると、ソフトウェアおよびサービスセグメントは、その専門性と効率性から特に高い成長を示すと予測されます。複雑なデータ管理、高度な分析、および規制遵守の専門知識が求められる中で、これらのセグメントはバイオ医薬品企業にとって不可欠なパートナーとなるでしょう。バリデーション機器・消耗品も、新しいセンサー技術や自動化ツールの進化により、継続的な需要が見込まれます。
最後に、持続可能性への意識の高まりも、**バイオプロセスバリデーション**の将来に影響を与える可能性があります。環境負荷の低減、資源の効率的な利用、廃棄物の削減といった側面が、製造プロセスだけでなく、バリデーション活動においても考慮されるようになるでしょう。これは、よりグリーンな製造プロセスとバリデーション手法の開発を促す可能性があります。これらの要因が複合的に作用することで、**バイオプロセスバリデーション**市場は、バイオ医薬品産業の持続的な成長と革新を支える重要な基盤として、今後もその存在感を高めていくことでしょう。
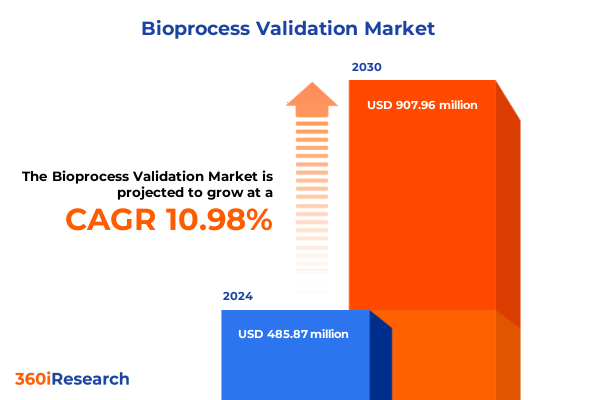
Table of Contents information not available.
*** 本調査レポートに関するお問い合わせ ***

バイオプロセスバリデーションは、バイオ医薬品の製造工程が意図した品質基準を満たす製品を一貫して生産できることを科学的かつ文書的に証明する、極めて重要な活動です。このプロセスは、患者の安全性、製品の有効性、そして品質を保証するために不可欠であり、医薬品規制当局が定める厳格な要件の根幹を成しています。複雑な生物学的システムを利用するバイオ医薬品の製造においては、原材料の変動性、細胞培養や精製プロセスの固有の複雑さから生じる潜在的なリスクを管理し、製造ロット間の均一性を確保することが最大の課題となります。
バリデーションの目的は、単に規制要件を満たすだけでなく、製造プロセスの深い理解を確立し、その制御状態を維持することにあります。これには、プロセス開発の初期段階から商業生産に至るまで、製品ライフサイクル全体にわたる継続的な取り組みが求められます。具体的には、重要なプロセスパラメータ(CPPs)と重要な品質特性(CQAs)を特定し、それらが適切に管理されていることを実証することが含まれます。例えば、細胞培養における温度、pH、溶存酸素濃度、培地の組成、あるいは精製工程におけるクロマトグラフィー条件などがCPPsに該当し、これらが最終製品の品質にどのように影響するかを評価します。
バイオプロセスバリデーションは多岐にわたる要素から構成されます。まず、設備・機器の適格性評価(IQ, OQ, PQ)は、製造に使用される全ての機器が正しく設置され、意図通りに機能し、期待される性能を発揮することを確認します。次に、洗浄バリデーションは、製造ラインの洗浄方法が効果的であり、前ロットの残留物や微生物汚染が次ロットに持ち越されないことを保証します。また、滅菌バリデーションは、無菌操作が必要な工程において、適切な滅菌条件が確立され、維持されていることを証明します。さらに、ウイルス除去・不活化バリデーションは、生物由来の原材料を使用する製品において、潜在的なウイルス汚染リスクを低減または排除するプロセスの能力を評価する上で極めて重要です。
分析法バリデーションもまた、製品の品質管理試験に使用される全ての分析法が、その目的に対して適切であることを保証するために不可欠です。これには、特異性、直線性、正確性、精度、検出限界、定量限界、範囲などのパラメータの評価が含まれます。これらの基礎的なバリデーション活動の上に、プロセス性能適格性評価(PPQ)が実施されます。PPQは、確立されたプロセスが、通常の製造条件下で一貫して高品質な製品を生産できることを、統計学的に有意なデータに基づいて実証するものです。これは通常、連続する複数の商業規模ロットの製造を通じて行われ、プロセスの頑健性と再現性を確認します。
近年では、Quality by Design (QbD) の概念がバリデーションアプローチに深く統合され、リスクベースのアプローチが主流となっています。これにより、製品品質に最も影響を与える要素に焦点を当て、リソースを効率的に配分することが可能になります。また、細胞・遺伝子治療製品のような新規モダリティの登場は、従来のバリデーション戦略に新たな課題を提示しており、より柔軟で適応性のあるアプローチが求められています。連続生産技術の導入もまた、バリデーションの考え方に変革をもたらしつつあります。
結論として、バイオプロセスバリデーションは、単なる規制遵守の義務ではなく、バイオ医薬品の品質、安全性、有効性を保証するための科学的基盤であり、患者の信頼を築く上で不可欠な要素です。これは、製品のライフサイクル全体にわたる継続的な品質保証活動の中核をなし、医薬品産業の持続的な発展を支える重要な柱であり続けます。